小腸腺がんに対し、世界に先駆けて抗体薬物複合体(ADC)を用いた第II相医師主導治験を開始
Press Release
2026年3月2日
小腸腺がんに対し、世界に先駆けて
抗体薬物複合体(ADC)を用いた第II相医師主導治験を開始
尿路上皮がんに対する既承認薬エンホルツマブ ベドチンが標的とする腫瘍抗原が
小腸腺がんでも高発現していることを発見した研究成果を臨床に展開
・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・・
2026年3月2日
国立研究開発法人国立がん研究センター
大阪国際がんセンター
九州大学病院
- 【発表のポイント】
-
・小腸腺がんは若年でも発症することがある希少がんで、一次治療の効果が得られなくなった患者さんの二次治療が確立されておらず、有効な治療法の開発が求められています。
・国立がん研究センター中央病院は、尿路上皮がんで承認されている抗体薬物複合体(ADC)のエンホルツマブ ベドチンが治療標的とする腫瘍抗原が、小腸腺がんでも同程度に発現していることを発見し、その結果を踏まえ本医師主導治験を計画しました。
・同研究成果は、エンホルツマブ ベドチンが小腸腺がんにも効果を示す可能性を示唆しており、エンホルツマブ ベドチンの小腸腺がんでの有効性と安全性を確認するため多施設共同第II相医師主導治験を開始しました。
・ADCは、がん細胞を選択的に攻撃する治療薬として、急速に研究開発が進んでおり、近年、固形がんに対する薬事承認が相次いでいます。小腸腺がんでADCを用いた治験は、世界に先駆けた取り組みであり、小腸腺がん治療の前進につながることが期待されます。
- 【概要】
-
国立研究開発法人国立がん研究センター(所在地:東京都中央区、理事長:間野 博行)中央病院(病院長:瀬戸 泰之)は、一次治療注1の効果が得られなくなった進行期小腸腺がんの患者さんを対象に第II相医師主導治験注2(ENVELOPE試験/NCCH2412試験)を実施します。
小腸腺がんは、若年でも発症することがある希少がん注3です。初期段階では症状が現れにくく、通常の内視鏡検査による早期発見が困難なため、診断時にはすでに進行していることが多い疾患です。外科的切除ができない進行期小腸腺がんに対しては、抗がん剤による全身化学療法が選択されますが、効果がある期間の中央値は約6か月程度で[1]、一次治療が効かなくなった後の二次治療注4は確立されていません。
国立がん研究センター中央病院では、小腸腺がんの新たな治療選択肢を開発するため、がん細胞を選択的に攻撃する抗体薬物複合体(Antibody–Drug Conjugate, 以下、ADC)注5に着目し、既承認薬が治療標的としている腫瘍抗原注6が小腸腺がんでも見られないか確認しました。その結果、尿路上皮がんの治療薬として承認されているADCであるエンホルツマブ ベドチンの治療標的腫瘍抗原であるネクチン-4(以下、Nectin-4)注7が、小腸腺がんでも高頻度に発現していることを発見しました[2]。同研究成果は、エンホルツマブ ベドチンが小腸腺がんにも効果を示す可能性を示唆しており、エンホルツマブ ベドチンの小腸腺がんでの有効性と安全性を確認するため、多施設共同第II相医師主導治験を開始しました。本医師主導治験では、より多くの小腸腺がんの患者さんが参加できるよう、国立がん研究センター中央病院(東京都)のほか、大阪国際がんセンター(大阪府)と九州大学病院(福岡県)でも実施します。
なお、本医師主導治験は、国立研究開発法人日本医療研究開発機構(AMED)の助成を受けて実施するもので、アステラス製薬株式会社から薬剤が無償提供されます。
- 【小腸腺がんについて】
-
私たちの体内にある「小腸」は、胃と大腸の間に位置し、長さが6〜7メートルにもなる臓器です。栄養素を吸収する役割を担い、消化器官全体の中でも約80%程度の非常に大きな部分を占めています。この小腸に発生するがんの一種が「小腸腺がん」です。小腸腺がんは全悪性腫瘍のうちの0.5%以下、全消化管悪性腫瘍のうちでも3%以下を占める極めて稀ながんです。欧米諸国からの報告では年間発症率は人口10万人あたり0.22〜0.57人とされ、一般的ながんに比べて患者数が極めて少ない希少がんに分類されます。
小腸腺がんは、およそ45%が十二指腸、35%が空腸、20%が回腸に生じます。このがんは初期には症状が現れにくく、また通常の内視鏡検査では観察しにくいため、診断される時には既に進行していることが多くあります。腸閉塞注8や腸管穿孔注9などの合併症を契機に発見されるケースも少なくありません。進行例では手術困難例も多く、たとえ手術ができたとしても、術後に再発するリスクは高いのが現状です。
現在、術後再発または外科的切除が困難な進行期の小腸腺がんに対し、唯一の薬物療法はFOLFOX(フォルフォックス)療法です。FOLFOXは大腸がんと胃がんでも用いられる併用化学療法で、小腸腺がんでも一定の有効性が報告されていますが、その効果持続期間の中央値はおよそ6か月にとどまります[1]。一次治療のFOLFOXが無効または副作用などで継続困難となった後に使用できる既承認薬はなく、二次治療以降の選択肢が乏しいことが小腸腺がん治療における大きな課題です。
- 【背景】
-
こうした状況を踏まえ、国立がん研究センター中央病院消化管内科を中心とした研究チーム(藤井博之、庄司広和、加藤健ら)は、新たな治療選択肢としてADCに着目しました。ADCは、がん細胞の表面にある特定の目印(腫瘍抗原)に結合するモノクローナル抗体に、強力な抗がん剤(ペイロード)を化学リンカーで結合させた薬剤です。腫瘍抗原に結合した後に細胞内へ取り込まれ、リンカーが切断されることで薬剤が放出され、がん細胞を直接攻撃します。腫瘍抗原を発現しない正常細胞への抗がん剤曝露が相対的に低くなるため、従来の殺細胞性抗がん剤と比べて正常組織への影響を抑えつつ高い有効性が期待されます。がん細胞を選択的に攻撃する「狙い撃ちの治療」として注目されており、近年、国内外で複数のADCが開発・実用化され、がん治療における重要な新規治療選択肢となりつつあります。
研究チームは、二次治療以降の選択肢が限られる小腸腺がん治療の現状を打開するため、既存あるいは開発中のADCを小腸腺がんの治療に応用できるか検討するため、ADCの標的となり得る複数の腫瘍抗原の発現を探索するトランスレーショナルリサーチ注10を実施しました。その結果、小腸腺がんにおいて、腫瘍抗原の一つであるNectin-4が約82%という高頻度で発現していることを明らかにしました[2]。このNectin-4を標的とするADCの一つがエンホルツマブ ベドチンであり、日本では「根治切除不能な尿路上皮癌」に対して承認されています。小腸腺がんにおけるNectin-4発現の頻度は、尿路上皮がんでの発現率と同程度であり、エンホルツマブ ベドチンが小腸腺がんにも効果を示す可能性があることを示唆しています。
この知見を踏まえて、国立がん研究センター中央病院では本医師主導治験を立ち上げました。
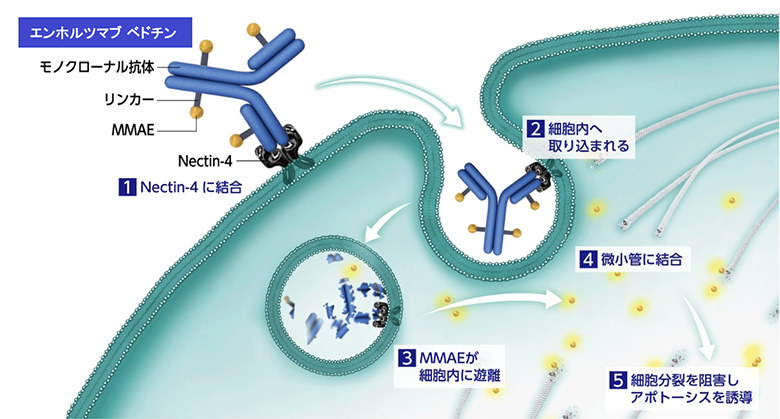
出典:アステラス製薬株式会社社内報告書一部改変:癌細胞(ヒト由来)・薬理作用(ヒトnectin-4への結合親和性)
図1 エンホルツマブ ベドチンは、がん細胞の細胞膜上に発現するNectin-4に結合し、細胞内に取り込まれた後にリンカーが切断され、MMAE(Monomethyl auristatin E;抗がん剤)が細胞内に遊離することでがんの増殖を抑制します。
- 【本医師主導治験について】
-
医師主導治験課題名
プラチナ併用療法に対して不応または不耐となった局所進行性または転移性の小腸腺癌患者を対象としたエンホルツマブ ベドチンを評価する多施設共同単群第II相医師主導治験
(ENVELOPE試験/NCCH2412試験)目的
本医師主導治験の主な目的は、エンホルツマブ ベドチンの小腸腺がん患者さんに対する有効性および安全性を評価することです。投与方法
エンホルツマブ ベドチンは点滴で体内に投与される抗がん剤です。28日を1コースとして、週1回の投与を3週間続けた後、4週目は休薬します。エンホルツマブ ベドチンが効かなくなったり副作用が出たりして投与が継続できなくなるまで投与を続けます。投与時には来院が必要になりますので、1か月に3回程度の来院が必要になります。対象となる患者さん(主な規準)
1.試験参加について、患者さんご本人から文書による同意が得られる
2.治験への登録時において、年齢が18歳以上
3.手術により切除ができない、または小腸周辺以外に広がっている、小腸腺がんと診断されている
4.以下のいずれかの抗がん剤治療を受け、効果がなくなった、または副作用で中止になった
-FOLFOX療法(フルオロウラシル+レボホリナート+オキサリプラチン)
-CapeOX療法(カペシタビン+オキサリプラチン)
5.遺伝子パネル検査などの結果によって推奨されている分子標的治療薬や免疫療法薬が無効、あるいは副作用で継続できない、あるいは合併症などで実施困難
6.各臓器機能が規定内に保たれている上記の規準は概要であり、記載した以外にも対象患者さんとなるための規準があります。上記に該当していても、本医師主導治験に参加できない場合がありますので、ご了承ください。
対象人数
本医師主導治験は、合計27人の患者さんにご参加いただくことを目標としています。医師主導治験実施医療機関
・国立がん研究センター中央病院
・大阪国際がんセンター
・九州大学病院医師主導治験調整医師(代表)
加藤 健(国立がん研究センター中央病院 頭頸部・食道内科/消化管内科 科長)臨床研究実施計画・研究概要公開システム
jRCT番号:jRCT2031250424
本医師主導治験の詳細は、以下よりご確認ください。
臨床研究実施計画・研究概要公開システム
URL:https://jrct.mhlw.go.jp/re/reports/detail/102835
- 【今後の展望】
-
本医師主導治験でエンホルツマブ ベドチンの小腸腺がんに対する有効性が示された場合、小腸腺がんの患者さんにとって全く新しい治療の選択肢となることが期待されるものであり、進行性または転移性の小腸腺がんに対する治療薬として薬事承認を目指します。
また、小腸腺がんの二次治療は、欧米を含む国際的な医療現場においても確立されておらず、本医師主導治験の成果は米国の治療ガイドラインなど、海外の診療指針に反映される可能性もあります。国際的にも注目される研究であり、将来的には国際共同研究グループとの連携を視野に入れ、さらなる治療法の開発を目指します。
- 【研究費】
-
●国立研究開発法人日本医療研究開発機構(AMED)
令和7年度革新的がん医療実用化研究事業
研究開発課題名:「プラチナ併用療法に対して不応又は不耐となった進行期小腸腺癌に対するEnfortumab Vedotinの単群第II相試験」
研究代表者名:加藤 健(国立がん研究センター中央病院 頭頸部・食道内科/消化管内科 科長)
- 【用語解説】
-
注1 一次治療
術後の再発もしくは進行期のがんと診断された際に、最初に行う化学療法。注2 医師主導治験
製薬会社ではなく、医師が主体となって薬の効果や安全性を確かめる臨床試験。注3 希少がん
『人口10万人あたり6例未満の「まれ」な「がん」、数が少ないがゆえに診療・受療上の課題が他に比べて大きいがん種』の総称。注4 二次治療
一次治療で効果が不十分だった場合や、副作用の観点から一次治療を中止した場合に、続けて行う次の治療。注5 抗体薬物複合体(Antibody–Drug Conjugate, ADC)
がん細胞特異的に結合する抗体と、強力な抗がん剤をリンカーで結合させた薬剤。抗体ががん細胞の表面に発現している標的抗原に結合すると、ADCは細胞内に取り込まれ、結合している抗がん剤が放出されてがん細胞を死滅させる。注6 腫瘍抗原
がん細胞の表面に特徴的に現れるタンパク質や糖鎖などの分子。正常な細胞にはほとんど見られない、あるいはごく少量しか発現していないが、がん細胞では発現量が増加するため、がん細胞を識別する目印のような役割を果たす。注7 ネクチン-4(Nectin-4)
細胞の表面にあるタンパク質の一つで、尿路上皮がんをはじめとした特定のがん細胞で特に多く見られる。この性質を利用してがんの標的治療に使われる。注8 腸閉塞
腸の中で食べ物や消化液が通れなくなり、腸の流れが止まってしまう状態。注9 腸管穿孔
腸の壁に穴が開いてしまい、腸の中の内容物が腹腔内に漏れ出す状態。注10 トランスレーショナルリサーチ
基礎研究で得られた成果を、実際の医療現場で使えるように応用していく研究。
- 【参考文献】
-
[1] Horimatsu T, Nakayama N, Moriwaki T, Hirashima Y, Fujita M, Asayama M, Moriyama I, Nakashima K, Baba E, Kitamura H, Tamura T, Hosokawa A, Yoshimura K, Muto M. A phase II study of 5-fluorouracil/L-leucovorin/oxaliplatin (mFOLFOX6) in Japanese patients with metastatic or unresectable small bowel adenocarcinoma. Int J Clin Oncol. 2017 Oct;22(5):905-912. doi: 10.1007/s10147-017-1138-6.
1)[2] Fujii H, Shoji H, Hirano H, Hirose T, Okita N, Takashima A, Kato K. Exploring novel therapeutic targets in small bowel adenocarcinoma: insights from claudin 18.2, nectin-4, and HER3 expression analysis. ESMO Open. 2025 Jan;10(1):104098. doi: 10.1016/j.esmoop.2024.104098.
- 【お問い合わせ先】
-
医師主導治験に関するお問い合わせ
国立研究開発法人国立がん研究センター中央病院
NCCH2412(ENVELOPE)医師主導治験調整事務局
Eメール:ncch2412_office@ml.res.ncc.go.jp広報窓口
国立研究開発法人国立がん研究センター企画戦略局 広報企画室
電話番号:03-3542-2511(代表)
Eメール:ncc-admin@ncc.go.jp大阪国際がんセンター 事務局 経営改革グループ
電話番号:06-6945-1181(代表)
Eメール:pr@oici.jp九州大学病院 総務課企画広報室
電話番号:092-642-5205
Eメール:ibskoho@jimu.kyushu-u.ac.jp
以上
【お問い合わせ先】
TEL 06-6945-1181(内線5107/5113/5118)
地方独立行政法人 大阪府立病院機構 大阪国際がんセンター
事務局 経営改革グループ
受付時間:平日9:00~17:30











