糖鎖オンコロジー部
スタッフ
| 谷口 直之 M.D., Ph,D. |
部長, (名誉研究所長) 大阪大学名誉教授 理研名誉研究員 https://researchmap.jp/read0013639 https://scholar.google.com/citations?user=7FUlYQ0AAAAJ&hl=en |
| 原田 陽一郎 Ph.D. |
大阪大学医学系研究科連携大学院分子腫瘍医学 客員教授 名古屋大学iGCORE研究所プロジェクト教授 https://researchmap.jp/harada_yoichiro |
| 大川 祐樹 Ph.D. |
チームリーダー 大阪大学医学系研究科連携大学院分子腫瘍医学 客員准教授 https://researchmap.jp/yohkawa |
| 岡本 三紀 Ph.D. |
チームリーダー |
| 栗原 大輝 Ph.D. |
研究員 https://researchmap.jp/taikikuribara |
| 阿部 純平 Ph.D. |
研究員 https://researchmap.jp/junpeiabe |
| 貫戸 紀子 | 実験補助員 |
| 藤縄 玲子 | 実験補助員 大阪大学医学系研究科連携大学院分子腫瘍医学 社会人学生 |
| 草川 美幸 | 事務補佐員 |
| Shi Yang | 大阪大学医学系研究科博士課程 |
| Wang Ziwei | 大阪大学医学系研究科博士課程 |
研究プロジェクト
N結合型分岐糖鎖に関わる糖転酵素の疾患での役割
糖鎖科学は、ゲノムやプロテオーム研究だけでは困難な様々な事実を明らかにできる代表的な研究分野である。糖鎖の変化が様々な疾患に深く関与していることは広く知られており、がんをはじめとする疾患における糖鎖発現の変化は、臨床診断のためのバイオマーカーや治療の指標として用いられている。また、インフルエンザやCOVID-19など、様々な感染症の発症にも糖鎖が関与している。さらに、糖転移酵素遺伝子(糖鎖遺伝子と呼ばれる)のノックアウトマウスを用いた基礎研究により、特異的な糖鎖付加が様々な疾患の発症因子であり、有望な治療標的であることが明らかになってきた。このような糖鎖科学の知見に基づき、当部門では、がんをはじめとする様々な疾患における糖鎖の基礎研究と臨床応用に力を入れている。
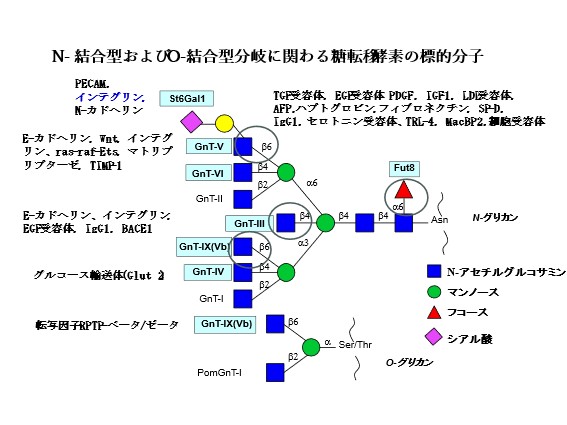
近年、加齢においても特定の糖鎖の変化が関与していることが報告されており(1)、糖鎖のさらなる理解は、現代の長寿社会における医学的課題を解決する上で重要である。具体的には、図中に円で囲ったbisecting GlcNAc(bisectと略す)、コアフコース、2つのβ1,6-GlcNAc分枝(β1,6分枝と略す、別々の酵素で作られる)と呼ばれるいくつかの糖鎖構造と、それらを合成する糖転移酵素とその遺伝子に注目した。これらの糖鎖の付加は、特定の糖タンパク質の糖鎖を構成し、がんの進行や転移に深く関与している(5-9)。特に、上皮間葉転換(EMT)や間葉上皮転換(MET)と呼ばれる現象や、その中間状態において、特異的な糖鎖を合成する遺伝子が、がんやがんの転移に強く関与していることが知られている(2)。さらに、糖鎖の修飾が、その中間体にも関与していることが知られている。このように、糖鎖とその誘導体は、がん、COPD、アルツハイマー病などの新たな創薬ターゲットとなる可能性が高いことを示してきた。がん細胞では、GnT-Vによるβ1,6分岐鎖の増加が、がんの転移と密接に関係している(3)(11)。逆にGnT-IIIによるbisect糖鎖の高発現は、がんの転移を抑制する。一方、脳においては、GnT-IIIの欠損がアルツハイマー病の原因であるアミロイドβ(Aβ)ペプチドの産生と脳内蓄積を激減させ、記憶力の低下を抑制することが示されており(4)(5)、そのメカニズムはAβ産生酵素であるBACE1の局在を変化させるというユニークなものであった(4)。また、コアフコース糖鎖においては、その発現量が各種がんの悪性度と正の相関を示すこと、コアフコースの欠損が肝臓癌の抑制効果を持つことを明らかにしている(6)。そしてそのメカニズムとして、コアフコースがEGF、PDGF、TGF-β、インテグリン、E-カドヘリンといった様々な成長因子受容体や接着分子の機能を調節することを明らかにしてきた(7-9)。近年、コアフコースは肝臓がん、非小細胞肺がん、膵臓がん、卵巣がん、前立腺がん、乳がん、甲状腺がん、メラノーマなどのがん組織で発現が上昇し、化学療法抵抗性にも関与していることが明らかになり、がんの新たな治療標的となっている。
分岐型N型糖鎖を生合成する糖転移酵素の標的分子の同定
私たちや他のグループによって、分岐型N型糖鎖を生合成する糖転移酵素の様々な標的分子が同定されている(下図を参照) (7, 8)。
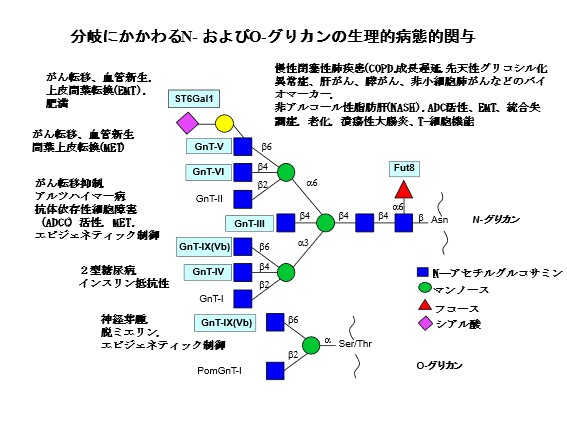
分岐型N型糖鎖および分岐型O型糖鎖を生合成する糖転移酵素とその生物機能
がんにおける細胞外小胞
私たちは、がん細胞から大量に分泌されるナノメートルサイズ(10億分の1メートル)の小さな袋状の物質である細胞外小胞(EV)の視点からも、がん研究を展開している。EVはがん細胞の増殖や転移を助けることから、がんの治療標的となりうる。我々は、がん細胞が好むグルコース誘導体(2-デオキシグルコース)が、がんの転移に関与するEVの分泌を抑制することを発見した(12-13)。この機構に糖鎖が深く関与していることから、糖鎖はがん転移の治療標的となる。がん細胞から分泌されるEVには、N型糖鎖をはじめ、がんの検出や診断に有用な情報が含まれており、我々は、EV中のN型糖鎖の構造を調べることで、肺がんの種類を診断できる可能性を見出している(9)。肺がんは、小細胞肺がんと非小細胞肺がんに分類され、それぞれ全く異なる特徴を持ち、治療法も異なる。現在の医療では、患者の体内から細胞を取り出して顕微鏡で見なければ、どちらかわからないが、細胞を取り出すには出血などの危険因子が伴う。EVは血液や尿などの体液に含まれており、患者の体液を使ったリスクの少ない診断法が期待される。
現在、前立腺がんには前立腺特異抗原(PSA)、消化器がんにはがん胎児性抗原(CEA)、卵巣がんにはCA125などの腫瘍マーカーがあることはよく知られており、その特異性は完全ではないにせよ、診断や治療の進展に有用なツールとして用いられている。一方、いわゆる早期がんや、将来がんになる可能性の高い前がん病変については、残念ながら決定的なバイオマーカーはほとんどない。最近、我々のグループは、IgGのコアフコース構造を特異的に認識するユニークなモノクローナル抗体を開発し、この抗体が肺がんや間質性肺炎の早期診断に有効である可能性を見出した(10)。今後さらに症例数を増やして結果を確認する予定であり、いわゆる早期がんや前がん病変に特異的なバイオマーカーを製品化するプロジェクトが進行中である。大川らは、間質性肺炎の場合、上記抗体が上記前癌病変を検出するバイオマーカーとなる可能性があることを報告している(10)。
当グループの新たな提案としての糖鎖レドックス(Glyco-Redox)研究
最近、2016年に国際的に提唱した研究領域である糖鎖レドックスに取り組んでいる(11) 生体内では生理的条件下において、活性酸素種(ROS)や活性窒素種(RNS)の生成系とその消去系がバランスよく機能している。当研究室では、酸化ストレスに関する研究を進め、酸化ストレス下における糖鎖の構造・機能と酸化還元制御システムとの関係を明らかにしてきた。実際、多くの糖鎖遺伝子やその制御因子が直接的あるいは間接的に糖鎖レドックスによって制御されており、がんの発生に関与している(12)。糖鎖レドックス研究の典型的な例として、活性酸素種消去酵素であるSOD3の1本の糖鎖が多様な機能を持つことを明らかにしてきた(13)。私たちは、このアプローチをがん、早期がん、前がん病変の新しい診断法や治療法に応用することをめざしている。
我々の研究に関連した糖鎖レドックス研究の概略図を下図に示す。
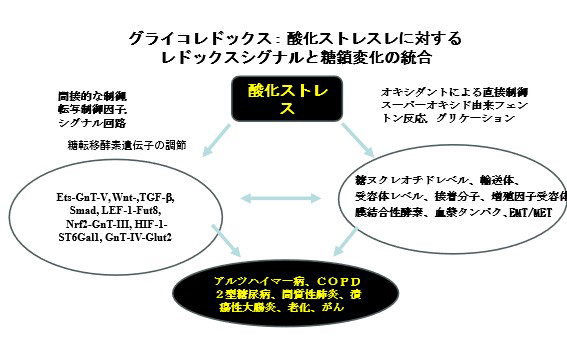
以上のように、糖鎖がその機能や代謝を変化させるメカニズムの解明は、がん、COPD、潰瘍性大腸炎、アルツハイマー病などに対する診断や治療法の開発、および糖鎖の発現や機能を阻害・模倣する糖鎖を用いた創薬への道を拓くものと期待される。このような糖鎖科学の経験と成果をもとに、現在、以下のような研究が進められている。
- 1) がん、炎症、COPD、間質性肺炎、脳機能における糖鎖の役割と制御に関する研究
- 2) がん、炎症、老化における糖鎖の役割と早期診断のための糖鎖バイオマーカーの探索に関する研究
- 3) 糖代謝に基づく新しいがん制御法の研究
現在、大阪大学大学院医学系研究科の大学院博士課程学生2名がこのプロジェクトに取り組んでいる - 4) 尿中などに含まれる遊離糖鎖構造のHPLCおよび質量分析法による解析、およびがんバイオマーカーへの応用に関する研究
- 5)新たながん制御法の創出を目指したケミカルバイオロジー研究(大阪大学大学院理学研究科・梶原康宏教授との共同研究)
References
- Vanhooren, V., Dewaele, S., Kuro, O. M., Taniguchi, N., Dollé, L., van Grunsven, L. A. et al. (2011) Alteration in N-glycomics during mouse aging: a role for FUT8 Aging Cell 10, 1056-1066
- Sasai, K., Ikeda, Y., Eguchi, H., Tsuda, T., Honke, K., and Taniguchi, N. (2002) The action of N-acetylglucosaminyltransferase-V is prevented by the bisecting GlcNAc residue at the catalytic step FEBS Lett 522, 151-155
- Taniguchi, N., Miyoshi, E., Ko, J. H., Ikeda, Y., and Ihara, Y. (1999) Implication of N-acetylglucosaminyltransferases III and V in cancer: gene regulation and signaling mechanism Biochim Biophys Acta 1455, 287-300
- Kizuka, Y., Kitazume, S., Fujinawa, R., Saito, T., Iwata, N., Saido, T. C. et al. (2015) An aberrant sugar modification of BACE1 blocks its lysosomal targeting in Alzheimer’s disease EMBO Mol Med 7, 175-189
- Kizuka, Y., Nakano, M., Kitazume, S., Saito, T., Saido, T. C., and Taniguchi, N. (2016) Bisecting GlcNAc modification stabilizes BACE1 protein under oxidative stress conditions Biochem J 473, 21-30
- Wang, X., Gu, J., Ihara, H., Miyoshi, E., Honke, K., and Taniguchi, N. (2006) Core fucosylation regulates epidermal growth factor receptor-mediated intracellular signaling J Biol Chem 281, 2572-2577
- Taniguchi, N., and Korekane, H. (2011) Branched N-glycans and their implications for cell adhesion, signaling and clinical applications for cancer biomarkers and in therapeutics BMB Rep 44, 772-781
- Taniguchi, N., and Kizuka, Y. (2015) Glycans and cancer: role of N-glycans in cancer biomarker, progression and metastasis, and therapeutics Adv Cancer Res 126, 11-51
- Kondo, Y., Harada, Y., Nakano, M., Suzuki, T., Fukushige, T., Hanzawa, K., Yagi, H. et al. (2023) Identification of distinct N-glycosylation patterns on extracellular vesicles from small-cell and non-small-cell lung cancer cells J Biol Chem 298, 101950
- Kanto, N., Ohkawa, Y., Kitano, M., Maeda, K., Shiida, M., Ono, T. et al. (2023) A highly specific antibody against the core fucose of the N-glycan in IgG identifies the pulmonary diseases and its regulation by CCL2 J Biol Chem 299, 105365
- Taniguchi, N., Kizuka, Y., Takamatsu, S., Miyoshi, E., Gao, C., Suzuki, K. et al. (2016) Glyco-redox, a link between oxidative stress and changes of glycans: Lessons from research on glutathione, reactive oxygen and nitrogen species to glycobiology Arch Biochem Biophys 595, 72-80
- Taniguchi, N., Ohkawa, Y., Kuribara, T., Abe, J., Harada, Y., and Takahashi, M. (2024) Roles of Glyco-Redox in Epithelial Mesenchymal Transition and Mesenchymal Epithelial Transition, Cancer, and Various Diseases Antioxid Redox Signal 41, 910-926
- Ohkawa, Y., Kitano, M., Maeda, K., Nakano, M., Kanto, N., Kizuka, Y. et al. (2023) Core Fucosylation Is Required for the Secretion of and the Enzymatic Activity of SOD3 in Nonsmall-Cell Lung Cancer Cells Antioxid Redox Signal 38, 1201-1211











