がん微小環境制御学部
スタッフ
| 坂上 倫久 | 部長 |
研究室紹介

腫瘍は単なるがん細胞の塊ではなく、炎症細胞や間質細胞、細胞外マトリクスなどから構成される複雑な腫瘍微小環境を形成しています。とりわけ、がん細胞は血管を介して酸素や栄養を獲得しながら増殖を続けますが、腫瘍内に形成される血管は、構造的・機能的に正常血管とは異なる「腫瘍血管」として特徴づけられます。当研究室では、腫瘍の進展や治療抵抗性に深く関与するこの腫瘍血管に着目し、新たながん治療戦略の開発を目指しています。
全身の血管をつなぎ合わせると地球約2周半に相当するとされ、血液循環ネットワークは体内の物質輸送に不可欠な基盤です。一般に、直径200 μmを超える組織の維持には血管による酸素・栄養供給が必須であり、この原理は異常増殖を示すがん細胞が腫瘍塊を形成する過程にも当てはまります。すなわち、腫瘍内微小循環の成立は、がん細胞の生存・増殖を支えるだけでなく、炎症細胞など腫瘍微小環境を構成する多様な細胞の供給にも重要な役割を果たします。
当研究室では、血管を構成する血管内皮細胞に着目し、臨床講座との連携のもと、臨床検体を用いた病態解析や血管構造を再現したがんオルガノイド培養系を活用して研究を進めています。これにより、腫瘍微小循環系の本質を分子・細胞レベルで解明するとともに、その制御を通じた新規がん治療法の確立を目指しています。現在、血管制御を基盤としたがん治療の開発に興味を持つ大学院生および研究員を広く募集しています。
テーマ1 細胞内タンパク質半減期制御を介したがん微小環境制御法の開発
腫瘍の増殖および転移には血管新生が不可欠であり、その制御機構の解明はがん治療における重要課題です。我々は、腫瘍血管新生が転写制御のみならず、細胞内タンパク質の半減期制御によって精緻に調節される点に着目してきました。一般的にゲノム情報をもとに転写されたmRNAの種類に比べて、翻訳されたタンパク質とその後に修飾されるタンパク質の種類は構造的にも機能的にも多様です。これまで我々は、この複雑な翻訳後修飾機構の中でも特にNEDD8化、ユビキチン・プロテアソーム系を介したタンパク質分解機構が血管新生関連因子の発現量および活性を規定することを明らかにしてきました(Ohnuki H et al., Blood. 2012;Miwa D et al., Angiogenesis. 2013;Sakaue T et al., Sci Rep. 2017;Sakaue T et al., Cancer Sci. 2017;Sakaue T et al., J Biochem. Review. 2017 Kovačević I and Sakaue T et al., J Cell Biol. 2018;Tanaka M et al., Arterioscler Thromb Vasc Biol. 2023)。
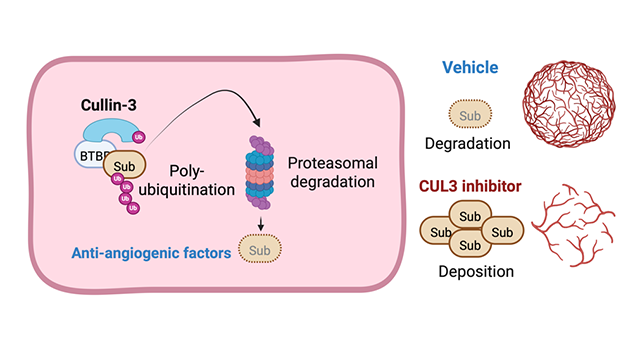
特に、Cullin-3をはじめとするE3ユビキチンリガーゼが、血管新生抑制因子の分解を介して血管新生を正に制御することを見出しています。現在は「血管新生抑制タンパク質の細胞内半減期制御による血管新生制御」をコンセプトに、次世代抗血管新生治療の開発を進めています。また、分解制御機構の操作による腫瘍血管正常化を通じて、がん進展抑制および治療効果向上を目指した新たな治療概念の確立にも取り組んでいます。さらに、細胞特異的かつ時期特異的なユビキチン修飾ダイナミクスを生体内で解析可能な遺伝子改変マウスを樹立しており、がんをはじめとするユビキチン修飾制御異常に起因する疾患の包括的理解を推進しています。
一方、NEDD8やユビキチンは細胞周期制御に関連したタンパク質に修飾され、細胞増殖に密接に関連しています。特に、NEDD8修飾阻害剤は急性骨髄性白血病の有望な治療薬として臨床研究がが進められています。我々の研究グループは固形腫瘍のみならず、臨床血液内科学分野と連携しながら、造血系と血液がん進展における翻訳後修飾機構のNEDD8化・ユビキチン化修飾シグナルの役割にも着目し、新たな抗がん剤開発に向けた基礎-臨床橋渡し研究も展開しています。
テーマ2 がん間質形成における血管新生の役割解明(JST創発的研究支援事業採択課題)
固形腫瘍においては、がん関連線維芽細胞や血管周皮細胞によって形成される腫瘍間質が、薬剤耐性やがん進展に深く関与することが知られています。我々の研究室では、血管新生に依存したがん間質形成を標的とした新たながん治療法の樹立を目指して研究を進めています。
これまで臨床胸部外科領域(循環器・呼吸器)と密接に連携し、がんをはじめとする外科治療後の重大な合併症である「術後組織間癒着」に着目し、その分子機構の解明に取り組んできました。独自に樹立した胸部癒着モデルマウスを用いた解析により、体腔損傷に伴って誘導される病的血管新生が、血管周囲に線維芽細胞や血管平滑筋細胞を集積させ、持続的な細胞外マトリックス産生を介して臓器間の癒着形成を促進することを明らかにしました(Kojima A et al., J Cardiotharacic Surg. 2019;Namiguchi K et al., Front. Cardiovasc. Med. 2022; Mori Y et al., Signal Transduct Target Ther. 2026)。
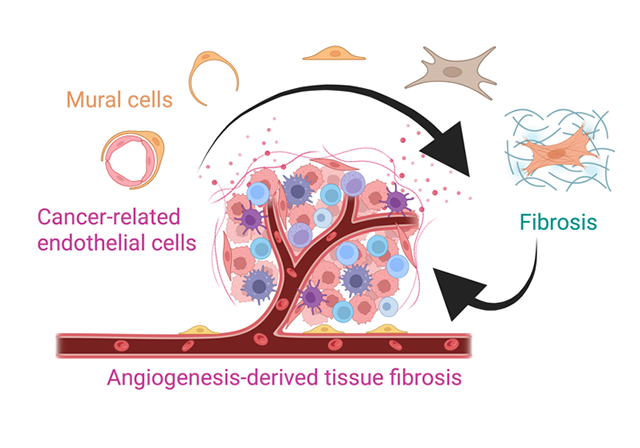
こうした線維化駆動性の病的血管新生は、本来組織が存在しない部位に新たな組織構造を形成するという点で、腫瘍微小環境の構築過程と本質的に共通する可能性があると考えています。この仮説に基づき、現在はがん間質形成と病的血管新生との関連性に着目した研究を展開しています。本研究では、血管新生と線維化のクロストークに焦点を当て、細胞間相互作用および細胞内シグナルネットワークの統合的理解を目指します。単一細胞解析や空間トランスクリプトミクスを活用し、がん間質形成過程における細胞動態と局所環境の変化を高解像度で可視化することで、新規がん治療標的分子の同定につなげます。さらに当研究室では、がん微小環境を構成する各種細胞において遺伝子改変が可能なマウスモデルを整備しており、血管内皮細胞を中心とした腫瘍微小環境構築の分子機構の解明と、その制御を基盤とした新規抗がん治療法の開発に取り組んでいます。
テーマ3 その他がん治療に関連した疾患治療の病態解明
近年、抗がん剤による心血管障害への理解の重要性が高まっており、特にアントラサイクリン系化学療法では、心不全や弁膜疾患の発症リスク増加が報告されています(Michael H, JACC Cardiovasc Imaging. 2016)。こうした背景のもと、我々は弁膜症で最も多い大動脈弁狭窄症の分子病態に着目して弁膜症に対する新規薬物治療法樹立に関する研究にも取り組んでおり、弁膜症発症には大動脈弁組織におけるカルシウム沈着、骨芽細胞分化関連遺伝子の発現上昇、さらには生体弁におけるマクロファージ集積が石灰化に関与することを明らかにしてきました(Sakaue T et al., Biol Open. 2018;Ann Thorac Surg. 2020;Kanno K et al., Int J Mol Sci. 2021)Sakaue T et al., JACC Basic Transl Sci. 2023)。また当部門では基礎研究成果を臨床応用へと橋渡しする国際的トランスレーショナルリサーチを様々な研究分野で推進しています。スペイン王国、米国、ベルギー、岡山大学、愛媛大学との国際共同研究では、臓器移植にて問題になる血管内皮細胞バリア破綻を起因とした虚血再灌流障害に関する病態解明を目指しています(Nakata K et al., Bioengineering. 2022;Kawana S et al., J Heart Lung Transplant. 2025;Okazaki M and Sakaue T et al et al., Arch Bronconeumol. 2025)。また、米国オハイオ州立大学と愛媛大学との連携のもと、がん治療後の組織欠損に対し、人工組織および医用デバイスを用いた再生治療戦略の開発も進めている(Kurobe H and Sakaue T et al., Sci Rep. 2026)。筑波大学や大分大学、岡山理科大学との連携では、血管新生誘導を主眼とした次世代組織再生医療技術の開発にも取り組んでいます。これは、がん治療などに関連した組織の損失を自己組織再生能力で補填するこれまでにない新たな試みです。当科では、これら国内外の共同研究基盤と最先端解析技術を融合し、臨床課題に直結した基礎研究を推進しています。得られた知見を創薬標的の同定や診断技術開発へと展開し、実臨床への還元を目指しています。基礎研究と臨床研究の双方向連携を強化することで、新たな医療価値の創出に貢献します。
※All figures were created by using BioRender.com (https://www.biorender.com).
論文
テーマ1
-
坂上倫久, 東山 繁樹.
血管新生研究 - 継往開来 -
血管. 48巻3号 p.129-138, 2025年 -
Habu K, Matsuoka Y, Hiyoshi H, Nakayama J, Watanabe K, Tate S, Sakaue T, Murai J, Uno K, Nishie H, Kubota E, Kataoka H, Joh T, Watanabe Y, Oshikiri T, Higashiyama S.
KLHL5 Contributes to Colorectal Cancer Cell Survival by Promoting Cell Cycle Progression and Suppressing Apoptotic Cell Death.
Cancer Sci. 116(9):2444–2456, 2025. -
Uno K, Nishie H, Hiyoshi H, Habu K, Nakayama J, Tate S, Sakaue T, Kubota E, Tanaka M, Shimura T, Kataoka H, Joh T, Higashiyama S.
Implication of KLHL Gene Family Member KLHL5 in Colorectal Cancer Progression and Prognosis.
Cancer Sci. 116(9):2580–2591, 2025. -
Tanaka M, Nakamura S, Sakaue T, Yamamoto T, Maekawa M, Nishinaka A, Yasuda H, Yunoki K, Sato Y, Sawa M, Yoshino K, Shimazawa M, Hatano M, Tokuhisa T, Higashiyama S, Hara H.
BCL6B Contributes to Ocular Vascular Diseases via Notch Signal Silencing.
Arterioscler Thromb Vasc Biol. 43(6):927-942, 2023. -
坂上倫久.
Cullin3 による新規血管新生制御機構.
月刊「細胞」. 11月号, 2018年 -
Kovačević I, Sakaue T (Co-first), Majoleé J, Pronk MC, Maekawa M, Geerts D, Fernandez-Borja M, Higashiyama S, Hordijk PL.
The Cullin-3-Rbx1-KCTD10 complex controls endothelial barrier function via K63 ubiquitination of RhoB.
J Cell Biol. 217(3):1015-1032, 2018. -
Nakayama H, Sakaue T, Maekawa M, Fujisaki A, Higashiyama S.
Cullin 3 regulates ADAMs-mediated ectodomain shedding of amphiregulin.
Biochem Biophys Res Commun. 499(1):17-23, 2018. -
Maekawa M, Tanigawa K, Sakaue T, Hiyoshi H, Kubota E, Joh T, Watanabe Y, Taguchi T, Higashiyama S.
Cullin-3 and its adaptor protein ANKFY1 determine the surface level of integrin β1 in endothelial cells.
Biol Open. 11:1707-1719, 2017. -
Sakaue T, Fujisaki A, Nakayama H, Maekawa M, Hiyoshi H, Kubota E, Joh T, Izutani H, Higashiyama S.
Neddylated Cullin 3 is required for vascular endothelial-cadherin-mediated endothelial barrier function.
Cancer Sci. 108:208-215, 2017. -
Sakaue T, Sakakibara I, Fujisaki A, Uesugi T, Nakashiro K, Hamakawa H, Kubota E, Joh T, Imai Y, Izutani H, Higashiyama S.
The CUL3-SPOP-DAXX axis is a novel regulator of VEGFR2 expression in vascular endothelial cells.
Sci Rep. 7:46915, 2017. -
Sakaue T, Maekawa M, Nakayama H, Higashiyama S.
Prospect of divergent roles of the CUL3 system in vascular endothelial cell function and angiogenesis.
J Biochem. 162:237-245, 2017. -
東山繁樹、坂上倫久、中山寛尚.
血管新生研究-血管の新生と退縮のバランス制御.
THE LUNG. vol.24, No1. メディカルレビュー社, 2016年 -
Miwa D, Sakaue T, Inoue H, Takemori N, Kurokawa M, Fukuda S, Omi K, Goishi K, Higashiyama S.
Protein kinase D2 and heat shock protein 90 beta are required for BCL6-associated zinc finger protein mRNA stabilization induced by vascular endothelial growth factor-A.
Angiogenesis. 16:675-688, 2013. -
Inoue H, Sakaue T, Ozawa T, Higashiyama S.
Spatiotemporal visualization of proHB-EGF ectodomain shedding in living cells.
J Biochem. 154(1):67-76, 2013. -
Ohnuki H, Inoue H, Takemori N, Nakayama H, Sakaue T, Fukuda S, Miwa D, Nishiwaki E, Hatano M, Tokuhisa T, Endo Y, Nose M, Higashiyama S.
BAZF, a novel component of cullin3-based E3 ligase complex, mediates VEGFR and Notch cross-signalling in angiogenesis.
Blood. 119(11):2688-2698, 2012
テーマ2
-
Mori Y, Sakaue T (Co-first), Okazaki M, Kurata M, Izutani H
Macrophage accumulations on the injured pulmonary surface promote intrathoracic adhesions
Signal Transduct Target Ther. 2026 in press -
Namiguchi K, Sakaue T (Co-first), Okazaki M, Kanno K, Komoda Y, Shikata F, Kurata M, Ota N, Kubota Y, Kurobe H, Nishimura T, Masumoto J, Higashiyama S, Izutani H.
Unique Angiogenesis From Cardiac Arterioles During Pericardial Adhesion Formation.
Front Cardiovasc Med. 8:761591, 2022. -
Nakao Y, Aono J, Hamaguchi M, Takahashi K, Sakaue T, Inoue K, Ikeda S, Yamaguchi O.
O-ring-induced transverse aortic constriction (OTAC) is a new simple method to develop cardiac hypertrophy and heart failure in mice.
Sci Rep. 12(1):85, 2022. -
Kojima A, Sakaue T (Co-first), Okazaki M, Shikata F, Kurata M, Imai Y, Nakaoka H, Masumoto J, Uchita S, Izutani H.
A simple mouse model of pericardial adhesions.
J Cardiothorac Surg. 14(1):124, 2019. -
Ahmat Amin MKB, Shimizu A, Zankov DP, Sato A, Kurita S, Ito M, Maeda T, Yoshida T, Sakaue T, Higashiyama S, Kawauchi A, Ogita H.
Epithelial membrane protein 1 promotes tumor metastasis by enhancing cell migration via copine-III and Rac1.
Oncogene. 37(40):5416-5434, 2018. -
Sakaue T, Shikata F, Utsunomiya K, Fukae S, Kurata M, Nakaoka H, Okazaki M, Kawanishi Y, Kojima A, Higashiyama S, Izutani H.
Proteomics-based analysis of lung injury-induced proteins in a mouse model of common bile duct ligation.
Surgery. 161:1525-1535, 2017. -
Shikata F, Sakaue T (Co-first), Nakashiro K, Okazaki M, Kurata M, Okamura T, Okura M, Ryugo M, Nakamura Y, Yasugi T, Higashiyama S, Izutani H.
Pathophysiology of lung injury induced by common bile duct ligation in mice.
PLoS One. 9(4):e94550, 2014.
テーマ3
-
Kurobe H, Sakaue T, Hirata Y, Moritani T, Kurata M, Higaki T, Shinoka T
Novel biodegradable device for transcatheter closure of atrial septal defects
Sci Rep. in press -
Kawana S, Okazaki M, Sakaue T, Hashimoto K, Nakata K, Choshi H, Tanaka S, Miyoshi K, Ohtani S, Ohara T, Sugimoto S, Matsukawa A, Toyooka S.
Loss of Nr4a1 ameliorates endothelial cell injury and vascular leakage in lung transplantation from circulatory-death donor.
J Heart Lung Transplant. 44(2):249-260, 2025. -
Okazaki M, Sakaue T, Tanaka S, Kubo Y, Hayashi T, Ramil E, Sánchez-López AJ, Coronado MJ, Hoyos L, Romero A, Toyooka S, Gomez-de-Antonio D.
Histological Features and Gene Expression Profiling in Lung Transplantation From Donation After Circulatory Death.
Arch Bronconeumol. S0300-2896(25)00003-1, 2025. -
Watanabe R, Kagimoto K, Chosei M, Sakaue T, Kurata M, Miura N, Kitazawa R, Kikugawa T, Higashiyama S, Saika T.
Vesicles Secreted by Renal Cell Carcinoma Cells Cause Vascular Endothelial Cells to Express PSMA and Drive Tumor Progression.
Cells. 14(3):165, 2025. -
Onji H, Tate S, Sakaue T, Fujiwara K, Nakano S, Kawaida M, Onishi N, Matsumoto T, Yamagami W, Sugiyama T, Higashiyama S, Pommier Y, Kobayashi Y, Murai J.
Schlafen 11 further sensitizes BRCA-deficient cells to PARP inhibitors through single-strand DNA gap accumulation behind replication forks.
Oncogene. 43(32):2475-2489, 2024. -
Yoshida S, Ikedo A, Yanagihara Y, Sakaue T, Saeki N, Imai Y.
Bub1 suppresses inflammatory arthritis-associated bone loss in mice through inhibition of TNFα-mediated osteoclastogenesis.
J Bone Miner Res. 39(3):341-356, 2024. -
Watanabe R, Liu S, Sakaue T, Ikegawa Y, Ohta M, Higaki T, Mogi M, Eguchi M.
Amelioration of oxygen-induced retinopathy in neonatal mice with fetal growth restriction.
Front Cell Dev Biol. 12:1288212, 2024. -
坂上倫久.
心血管系の恒常性を維持する大動脈弁の役割と弁石灰化メカニズム
医学のあゆみ. 289巻13号 p.1112-1116, 2024年 -
Takahashi K, Aono J, Nakao Y, Hamaguchi M, Suehiro C, Kurata M, Sakaue T, Kakino A, Sawamura T, Inoue K, Ikeda S, Suzuki J, Yamaguchi O.
LOX-1 deficiency increases ruptured abdominal aortic aneurysm via thinning of adventitial collagen.
Hypertens Res. 46(1):63-74, 2023. -
Kato H, Saeki N, Imai M, Onji H, Yano A, Yoshida S, Sakaue T, Fujioka T, Sugiyama T, Imai Y.
LIM1 contributes to the malignant potential of endometrial cancer.
Front Oncol. 13:1082441, 2023. -
Sakaue T, Koyama T, Nakamura Y, Okamoto K, Kawashima T, Umeno T, Nakayama Y, Miyamoto S, Shikata F, Hamaguchi M, Aono J, Kurata M, Namiguchi K, Uchita S, Masumoto J, Yamaguchi O, Higashiyama S, Izutani H.
Bioprosthetic Valve Deterioration: Accumulation of Circulating Proteins and Macrophages in the Valve Interstitium.
JACC Basic Transl Sci. 8(7):862-880, 2023. -
Sakaue T, Izutani H.
Reply: Low-Grade Inflammation: A Familiar Factor in Cardiovascular Diseases.
JACC Basic Transl Sci. 8(11):1476, 2023. -
Nakata K, Okazaki M, Sakaue T, Kinoshita R, Komoda Y, Shimizu D, Yamamoto H, Tanaka S, Suzawa K, Shien K, Miyoshi K, Yamamoto H, Ohara T, Sugimoto S, Yamane M, Matsukawa A, Sakaguchi M, Toyooka S.
Functional Blockage of S100A8/A9 Ameliorates Ischemia-Reperfusion Injury in the Lung.
Bioengineering (Basel). 9(11):673, 2022. -
Nakayama H, Ohnuki H, Nakahara M, Nishida-Fukuda H, Sakaue T, Fukuda S, Higashiyama S, Doi Y, Mitsuyoshi M, Okimoto T, Tosato G, Kusumoto C.
Inactivation of axon guidance molecule netrin-1 in human colorectal cancer by an epigenetic mechanism.
Biochem Biophys Res Commun. 611:146-150, 2022. -
Higashi H, Iio C, Ikeda S, Uetani T, Inaba S, Inoue K, Sakaue T, Izutani H, Yamaguchi O.
Huge Right Coronary Artery Aneurysm in Mixed Connective Tissue Disease.
Circ J. 86(5):881, 2022. -
Kanno K, Sakaue T, Hamaguchi M, Namiguchi K, Nanba D, Aono J, Kurata M, Masumoto J, Higashiyama S, Izutani H.
Hypoxic Culture Maintains Cell Growth of the Primary Human Valve Interstitial Cells with Stemness.
Int J Mol Sci. 22(19):10534, 2021. -
Higashi H, Nishimura T, Aono J, Sakaue T, Kurata M, Izutani H, Yamaguchi O.
Pathological Evidence of Native Aortic Valve Injury After Impella Support.
Circ Heart Fail. 14(2):e007571, 2021. -
Akazawa Y, Inaba S, Sakaue T, Kurata M, Aono J, Yasugi T, Moritani T, Nishiyama H, Higaki T, Eguchi M, Yamaguchi O.
Active aneurysm thrombosis after Kawasaki disease in an adult: Insight into anticoagulation therapy.
J Cardiol Cases. 23(5):206-209, 2020. -
Sakaue T, Hamaguchi M, Aono J, Nakashiro KI, Shikata F, Kawakami N, Oshima Y, Kurata M, Nanba D, Masumoto J, Yamaguchi O, Higashiyama S, Izutani H.
Valve Interstitial Cell-Specific Cyclooxygenase-1 Associated With Calcification of Aortic Valves.
Ann Thorac Surg. 110(1):40-49, 2020. -
Ahmat Amin MKB, Shimizu A, Zankov DP, Sato A, Kurita S, Ito M, Maeda T, Yoshida T, Sakaue T, Higashiyama S, Kawauchi A, Ogita H.
Epithelial membrane protein 1 promotes tumor metastasis by enhancing cell migration via copine-III and Rac1.
Oncogene. 37(40):5416-5434, 2018. -
Inoue Y, Shimazawa M, Nakamura S, Takata S, Hashimoto Y, Izawa H, Masuda T, Tsuruma K, Sakaue T, Nakayama H, Higashiyama S, Hara H.
Both autocrine signaling and paracrine signaling of HB-EGF enhance ocular neovascularization.
Arterioscler Thromb Vasc Biol. 38:174-185, 2018. -
Sakaue T, Nakaoka H, Shikata F, Aono J, Kurata M, Uetani T, Hamaguchi M, Kojima A, Uchita S, Yasugi Y, Higashi H, Suzuki J, Ikeda S, Higaki J, Higashiyama S, Izutani H.
Biochemical and histological evidence of deteriorated bioprosthetic valve leaflets: the accumulation of fibrinogen and plasminogen.
Biol Open. 7(8):bio034009, 2018. -
Nishida-Fukuda H, Araki R, Shudou M, Okazaki H, Tomono Y, Nakayama H, Fukuda S, Sakaue T, Shirakata Y, Sayama K, Hashimoto K, Detmar M, Higashiyama S, Hirakawa S.
Ectodomain shedding of Lymphatic Endothelial Hyaluronan Receptor 1 (LYVE-1) is induced by VEGF-A.
J Biol Chem. 291:10490-10500, 2016. -
Inoue H, Sakaue T, Ozawa T, Higashiyama S.
Spatiotemporal visualization of proHB-EGF ectodomain shedding in living cells.
J Biochem. 154(1):67-76, 2013.











